

1.Einleitung 2.Grundlagen 3.Adsorptions-Isothermen 4.Mehrkomponenten-Adsorption 5.Aktivkohlefilter
Da in der Praxis meist nicht nur eine, sondern mehrere Komponenten aus einem Luftgemisch zu adsorbieren sind, hat die Mehrkomponenten-Adsorption für die Praxis eine große Bedeutung. Die grundsätzlichen Zusammenhänge bleiben dabei bestehen, werden aber durch die unterschiedlichen Bindungkräfte der einzelnen Stoffe recht komplex.
Bei der Mehrkomponenten-Adsorption konkurrieren die verschiedenen Stoffe um die Adsorptionsplätze in der Aktivkohle. Dies hat zur Folge, daß sich die Beladung für die Einzelkomponenten bei der simultanen Adsorption anderer Stoffe erniedrigt. Die Beladung ist um so geringer, je besser die anderen Stoffe adsorbierbar sind.
Die Berechnung der gegenseitigen Beeinflussung bei der Mehr- komponenten-Adsorption erfolgt mit Hilfe der Theorie der ideal adsorbierten Lösung (IAST). Sie erfordert die Kenntnis der Einzelisothermen der beteiligten Stoffe und der Gemischzusammensetzung. Im Rahmen dieser Arbeit kann hier nicht näher auf Einzelheiten eingegangen werden. Diese findet man bei KAST (1988: S. 56 ff).
Hier sollen nur beispielhaft die Adsorptions-Isothermen für das in der Praxis häufig anzutreffende CKW-Gemisch Tetrachlorethen - cis 1,2 Dichlorethen (Per - Cis) skizziert werden. Per ist ein Stoff der sehr gut an Aktivkohle adsorbiert wird, Cis dagegen relativ schlecht. In Abb. 9 sind die Isothermen von Cis bei vier verschiedenen Per-Konzentrationen aufgetragen. Man erkennt, daß die Beladung der Kohle mit Cis durch die gleichzeitige Anwesenheit von Per stark reduziert wird. So beträgt die Beladung der Kohle mit Cis bei 100 mg/m³ Cis ohne Per etwa 3 Gew.-%, bei Anwesenheit von zusätzlich 500 mg/m³ Per aber nur etwa 0,5 Gew.-%.
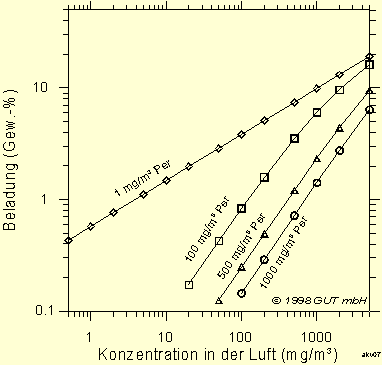
Abb. 9: Adsorptions-Isothermen (20 °C) von cis 1,2 Dichlorethen bei Anwesenheit von Tetrachlorethen (Per). Berechnet nach IAST
Die Adsorption von Per wird durch Cis dagegen nur relativ wenig behindert. Abb. 10 zeigt, daß die Beladung mit Per bei 100 mg/m³ Per ohne Cis etwa 22 Gew.-% beträgt. Kommen noch 500 mg/m³ Cis dazu reduziert sich die Beladung lediglich auf etwa 20 Gew.-%.
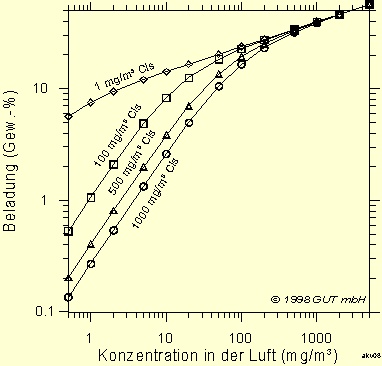
Abb. 10: Adsorptions-Isothermen (20 °C) von Tetrachlorethen
bei Anwesenheit von
cis 1,2 Dichlorethen (Cis). Berechnet nach IAST.
Aktivkohle verhält sich hydrophob, d.h. sie adsorbiert Wasser nur relativ schlecht. Sie ist deshalb, im Vergleich mit anderen Adsorbentien wie z.B. Silicagel, besonders für die Reinigung von feuchter Luft geeignet, da der Wasserdampf die Adsorption der Schadstoffe nur relativ wenig behindert, obwohl Wasserdampf, in der Regel mit Konzentrationen zwischen 5.000 und 20.000 mg/m³, die Hauptkomponente bei der Luftreinigung darstellt.
Die Adsorptions-Isotherme von Wasser ist in Abb. 11 graphisch dargestellt. Man erkennt, daß die Beladung bei trockener Luft nur wenige Prozent beträgt. Erst bei relativen Luftfeuchtigkeiten um 50 % steigt die Beladung in Folge von Kapillarkondensation (Kondensation unter dem Siedepunkt in engen Kapillaren) steil an.
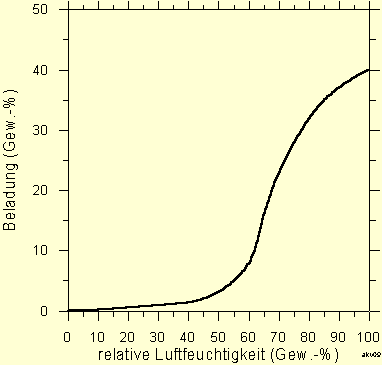
Abb. 11: Adsorptions-Isotherme (25 °C) von Wasserdampf in Luft
Die Auswirkung der Luftfeuchtigkeit auf die Adsorption von organischen Schadstoffen ist am Beispiel Benzol in Abb. 12 graphisch dargestellt. Bei trockener Luft beträgt die Beladung mit Benzol 16 Gew.-%, bei einer Luftfeuchtigkeit von 50 % immerhin noch 14 Gew.-%, bei sehr feuchter Luft (90 %) aber nur noch 4 Gew.-% Benzol.
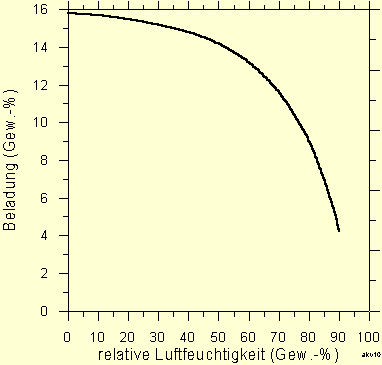
Abb. 12: Der Einfluß der Luftfeuchtigkeit auf die Adsorption von Benzol (170 mg/m3, 25 °C, nach Lurgi)
Solange die relative Luftfeuchtigkeit also unter 50 % liegt, wird die Adsorption der organischen Schadstoffe nur wenig beeinträchtigt. Da die aus dem Boden abgesaugte Luft meist nahezu mit Wasserdampf gesättigt ist, muß sie für eine effektive Adsorption etwas getrocknet werden. Dies geschieht in der Praxis mit einer leichten Temperaturerhöhung.
Daß die Adsorption von organischen Schadstoffen durch hohe Wasserkonzentrationen stark beeinträchtigt werden kann, wird im Extremfall bei der Reinigung von Wasser deutlich. Abbildung 13 zeigt dazu die Isothermen von Tetrachlorethen bei der Reinigung von Luft im Vergleich zu der Reinigung von Wasser. Bei einer Per-Konzentration von 100 mg/m³ erzielt man bei der Reinigung von Luft eine Beladung von etwa 22 %, bei der Reinigung von Wasser aber nur etwa 6 %.
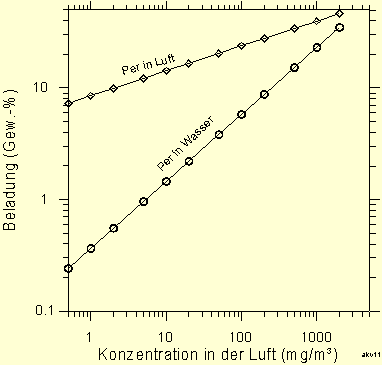
Abb. 13: Adsorptions-Isothermen (20 °C) von Tetrachlorethen (Per) in Wasser und in Luft
Bei der Reinigung von Grundwässern spielt die Mehrkomponenten-Adsorption darüberhinaus eine weitere bedeutende Rolle, da in jedem Grundwasser natürlicherweise eine Reihe von organischen Stoffen vorkommt, die unter dem Namen Huminstoffe zusammengefaßt werden können. Diese Huminstoffe werden recht gut von Aktivkohle adsorbiert und vermindern somit die Beladung mit den organischen Schadstoffen. Die oben genannten 6 % Beladung unter idealen Bedingungen reduzieren sich in der Praxis dadurch auf unter 1 % (siehe unten).
Bei der Adsorption stellt sich nach hinreichend langer Zeit ein stationärer Zustand bei der Konzentration auf der Kohle und im Fluid ein, den man als Adsorptionsgleichgewicht bezeichnet. Die Adsorptionskinetik beschreibt die Geschwindigkeit, mit der sich das System dem Gleichgewicht nähert.
Der Adsorptionsvorgang besteht aus einer Reihe von Transportvorgängen. Das Schadstoffmolekül muß zunächst an das Aktivkohlekorn herantransportiert werden und dann von der Kornoberfläche weiter in das Korninnere diffundieren. Korngröße und Porenstruktur beeinflussen in starkem Maße die kinetischen Eigenschaften der Aktivkohle. Je kleiner die Aktivkohlepartikel sind, desto schneller wird der Schadstoff adsorbiert. Daraus resultiert die Anwendung von Pulverkohle (Einrühren in Wasser und später abfiltrieren). Um die langsame Adsorptionsgeschwindigkeit der großen Aktivkohlepartikel der Kornkohle auszugleichen wird in den Festbett-Adsorbern viel Kohle mit wenig Wasser oder Gas in Kontakt gebracht (hohe Aktivkohle-Konzentration).
Wegen der hohen Beweglichkeit dampfförmiger Moleküle sind Adsorptionsvorgänge aus der Gasphase nach etwa 1 Sekunde im Gleichgewicht. Bei der Adsorption aus dem viskoseren Wasser dauert die Einstellung des Gleichgewichts dagegen einige Minuten.
Bei höherer Temperatur wird das Gleichgewicht schneller erreicht, die Beladung ist dann allerdings geringer. Bei der Adsorption wird Wärme frei.